施国海医生的科普号
- 精选 为了病人的一切,谈保留肾脏手术的再认识
T1期肾癌的5年无疾病复发的生存率可以达到92%,而国人T1期肾癌患者中慢性肾病的比例为25%,老年人可能达到60%,这些术后长期存活,肿瘤控制很好的患者,如何保肾,减少后续的代谢性疾病的发生是目前肿瘤治疗的难点和要点!我们希望通过改善手术技巧,开展新的手术方式如消融,纳米刀等方式,尽可能的为患者考虑5年,10年甚至30年后的问题,是我们义不容辞的迫切任务!
施国海 主任医师 复旦大学附属肿瘤医院 泌尿外科3840人已读 - 精选 前列腺癌确定性治疗的现状与展望
前列腺癌(prostate cancer , PCa)是男性最常见的恶性肿瘤之一 ,2006 年排名美国男性癌症死因的第2位 ,在我国正呈快速增长趋势。PCa 的确定性治疗手段包括根治性前列腺切除术和放射治疗 ,放射治疗主要方式有常规体外照射、 中子照射以及短时间或永久性组织间插植放疗。目前 , PCa 的确定性治疗方法是根治性前列腺切除术、 体外放射治疗和放射性同位素永久性插植治疗。根据现有资料 ,在预后因素相似的患者中 ,3 种治疗方法所获得的无 PSA 复发生存率和无病生存率差异无统计学意义[1 ]。1 根治性前列腺切除术1. 1 手术适应证根据 AJ CC 和 UICC 的 TNM 分期系统 ,可以将前列腺肿瘤分为局限早期、 局部晚期和晚期。局部早期 PCa ( T1~T2 期)是根治性前列腺切除术的绝对适应证。对于 T3 期(肿瘤已穿透包膜 ,有精囊或局部侵犯)患者是否应行 PCa 根治术一直存在争议。有学者认为 ,手术后切缘阳性、 淋巴结转移或远处转移的发生率都高于局部早期 PCa ,因此 ,很多 T3 期患者接受内分泌治疗或者放射治疗 + 内分泌治疗。然而 ,Ward等[2 ]观察 842 例接受 PCa 根治术的 T3 期患者 ,10 和15 年的生存率分别为 90 %和 79 % ,需要指出:这组患者中有 1/ 2 接受了辅助内分泌治疗。Carver 等[3 ]报道 ,176 例临床 T3 期患者接受 PCa 根治术后随访 614年 ,结果 52 %无生化或临床复发;进展到生化复发的中位时间为 416 年。虽然有 1/ 3 患者接受 3~4 个月的新辅助治疗 ,但不能作为预测生化复发的依据。5、10 和 15 年 PCa 的死亡率分别为 6 %、 15 %和 24 %。Step hen等[4 ]报道了单纯 PCa 根治术后长期肿瘤控制率的比例约为 50 % ,癌相关生存率为 84 %。长期随访发现 ,短期新辅助治疗方法虽可降低患者切缘阳性率 ,但对于患者长期预后均无明显改善 ,且新辅助治疗方法具有激素治疗的不良反应 ,并且增加患者费用 ,辅助治疗的确切疗效尚需更大样本、 更长随访时间的临床随机试验来证实。J ennifer 等[ 5 ]报道 ,患者肛门指检(DRE)明显异常并且 Gleason 评分高达 9 分 ,并且 MRI和 DRE 都提示肿瘤侵犯血管神经束 ,术中也发现肿瘤侵犯血管神经束,行双侧保留血管神经束的手术的患者切除狄氏筋膜包括直肠前壁脂肪 ,也达到完整切除肿瘤的目的。> 1/ 2 的患者术后切缘阴性 ,无生化复发。尽管对前列腺侵犯程度目前尚无可靠的诊断手段 ,但是术前 MRI对于外科医生决定治疗方案尤为重要。对于T3 期患者根治术后可行辅助性内分泌治疗和放疗 ,主要适用于高危患者及术后发现前列腺包膜或精囊侵犯、 切缘阳性或淋巴阳性者。多数学者建议术后早期内分泌治疗 ,但尚未能证明早期内分泌治疗能够提高生存率。术后放疗可提高无进展生存期 ,减少局部复发 ,但尚无证据提示放疗可提高远期生存率。有报道 ,C期病变因切缘阳性、 肿瘤已穿透包膜及精囊受侵犯等因素做术后放疗者 ,5 年局部控制率为 80 % ,10 年为 72 %。根治性前列腺切除术后有复发者做放疗也可得到很好的局部控制。虽然 PCa 根治术不存在严格的年龄限制 ,但是随着年龄的增加 ,并发症的发生率明显增加 ,尤其是 > 70岁的患者死亡风险会增加。1. 2 淋巴结清除盆腔淋巴结清除术是判断淋巴结转移和决定分期最准确的手段 ,同时也为术后辅助治疗和判断预后提供依据。高危局限性 PCa 患者和微小病灶转移的患者通过盆腔淋巴结清除得到最大收益 ,而对于淋巴结广泛转移的患者则可能从雄激素剥脱治疗中收益[6 ]。目前认为 ,淋巴结阳性即意味着全身转移 ,提示预后较差且需要系统治疗,但遗憾的是至今尚无特异性检测方法决定淋巴结转移情况。目前多数学者认为 , PSA< 10 ng/ mL , Gleason 评分 < 7 的患者淋巴结转移的发生率较低 ,不主张行淋巴结清除术 ,但这可能低估了淋巴结转移的发病率。对于 PSA < 10 ng/ mL , Gleason评分 > 7 的患者 ,淋巴结转移的阳性率为 25 %,建议行淋巴结清除术。淋巴结造影术显示 ,前列腺淋巴引流不止局限于闭孔和髂外血管 ,还包括髂内和骶骨前淋巴结。广泛的淋巴结清除术(lymp h node dissection ,LND) ,一般多于 20 个淋巴结 ,而局限性的 LND ,平均只有 8~10个淋巴结。但广泛的淋巴结清除与局限性清除术相比 ,并发症发生率增加,如淋巴囊肿、 淋巴管水肿及深静脉血栓等。1. 3 新的手术方式开放 PCa 根治术、 腹腔镜 PCa 根治术和机器人辅助 PCa 根治术在术中和术后并发症发生率方面并无较大差别;失血量和住院时间方面腹腔镜 PCa 根治术和机器人辅助 PCa 根治术还具有优势[7 ]。机器人辅助 PCa 根治术具有微创、 学习曲线短等优点 ,英国一中心报道 ,机器人辅助 PCa 根治术的时间 ,前 15 例平均需 355 min , 而后15例 的平均时间只需 要256 min[8]。腹腔镜 PCa 根治术和机器人辅助 PCa 根治术的学习曲线略有不同 ,在北美有逐步取代腹腔镜PCa 根治术的趋势。1. 4 新辅助内分泌治疗与 PCa 根治术PCa 患者术前准确的临床分期较为困难 ,文献报道 ,42 %~50 %的患者术前分期被低估 ,根治性前列腺切除术后 ,手术切缘阳性率及包膜外受侵率高达25 %。因此 ,有些学者提出了新辅助治疗的概念 ,以期减少肿瘤的体积、 降低肿瘤的分期并抑制潜在的转移发生 ,达到使手术切除彻底、 提高治愈率的目的。新辅助内分泌治疗不能提高 PCa 根治术的总体生存率 ,不能延长无疾病生存期 ,而且可能耽搁手术治疗的最佳时间。其远期疗效还需要进一步研究。2 体外放射治疗放疗的优势与根治性手术相比创伤性小 ,术后尿失禁勃起功能障碍的发生率低。对于早期肿瘤的治疗效果与根治术类似 ,使 80 %~90 %的 T1 、 T2 期 PCa得到控制。但是由于前列腺仍留在体内 ,增加了肿瘤复发的可能。尽管保护周围正常的组织 ,患者还可能会发生肠道、 尿道和生殖系统损伤。放疗后的局部控制率与肿瘤的临床分期、 分化程度、 肿瘤大小、 照射剂量和照射野的大小等因素有关。体外照射(externalbeam radiation t herapy ,EBRT)范围通常包括前列腺、双侧精囊、 前列腺周围组织和盆腔淋巴结 ,照射剂量60~70 Gy。单独应用 EBRT的 5 年无复发生存率为30 %~50 % ,联合抗雄激素治疗能够使其升高至50 %~85 %。EBRT与 PCa 根治术和内放射相比 ,没有解剖结构上限制 ,治疗范围较大。低危患者应用> 70 Gy的放射治疗能够减少 PSA 复发的风险 ,但是对生存期无显著作用;对于高危患者 ,外放射治疗加激素治疗( > 3 年)能够延长生存时间。而间歇性放射治疗(70 Gy)配合新辅助或同时给予激素治疗 6 个月能够延长生存时间。RTOG 85231 试验报道 ,977 例临床 T3 期或伴有淋巴结转移的患者 ,中位随访时间为716 年 ,联合治疗(放疗 +化疗)后 ,只有 < 25 %的患者死于 PCa[9 ]。短期的内分泌治疗能够提高放射效果。内分泌治疗对大多数中晚期 PCa 患者有明确的疗效 ,内分泌治疗后肿瘤体积明显缩小甚至消失 ,放疗与其结合可提高中晚期 PCa 的控制率。美国 RTOG对 ⅡB 期和 C期 PCa 患者进行前瞻性随机分组临床研究以确定内分泌治疗和体外放疗的疗效 ,结果显示 ,综合治疗组较单纯应用放射治疗组的 4 年局部失败率、 远处转移率、无病生存率和生化无病率均显示了显著的优势。新的放射技术如三维适形放疗、 调强技术逐渐应用到临床中。回顾性研究显示 , PCa 照射剂量的增加不仅提高了无生化复发生存率 ,同时提高了总生存率。由于前列腺紧邻直肠、 膀胱 ,常规放疗剂量通常≤70 Gy。20 世纪 90 年代开展的三维适形放疗(3DCRT) 技术可使靶区剂量提高到 78 Gy 甚至> 80 Gy ,降低了放疗后 PCa 活检阳性率,提高了局部控制率,显著改善 PCa 无生化失败生存率;同时 ,因三维形状的适合度大大提高 ,显著减少周围正常组织和器官受照体积 ,在照射剂量提高的同时并未增加直肠和膀胱不良反应。质子和重离子与传统光子(X线)相比具有更好的剂量分布 ,靶区适形度好 ,能更好地保护直肠 ,降低直肠损伤。一项临床 Ⅲ期随机对照试验报道 ,试验组(103 例) 光子适形照射 5014 Gy , 质子加量到6715 Gy ;对照组(99 例)常规放疗技术。结果试验组5 和 8 年局控率分别为 94 %和 84 % ,对照组分别为64 %和19 % , P = 01001 4。治疗后 8 年直肠出血率 ,试验组32 % ,对照组 12 % ,两组的出血都较轻 ,没有严重后遗症。治疗效果优于光子立体适形放疗 ,甚至好于手术治疗 ,放疗后的并发症也不严重。5 和 10 年后≥GTOG 3 级消化道和泌尿道毒副反应发生率均为1 %[10 ]。Loma Linda 用质子放疗 PCa 的经验为:采用70~250 MeV 同步加速器 ,对高危转移者( Partin nomogram , ≥ 15 % DM)给予光子 45 Gy (原发灶 +第 1、2 站淋巴引流区) ,质子 30 CGE/ 15f x 加量原发灶;对低危转移者 ,质子74 CGE/ 37f x 714wks (前列腺、 精囊小体) 5 mm 边界。碳离子放疗的技术已应用在 PCa( T1b~T3 )的患者 ,取得了极好的疗效 ,而且没有明显的毒副反应 ,但还需进一步研究证实[11 ]。3 组织间插植放疗1981 年 ,Holm等采用经直肠超声引导下经会阴前列腺穿刺 ,将放射性核素125I粒子植入治疗 PCa。此后 ,治疗计划系统( TPS)的开发使放射性粒子在前列腺内分布更加合理 ,至今在欧美国家得到广泛应用。由于近距离放射治疗可使肿瘤局部达到高剂量照射 ,而对周围正常组织影响较少 ,明显提高了临床效果 ,降低了并发症的发生率 ,在国外已成为治疗局限性 PCa的重要手段之一。其适应证与根治术相似 ,主要适用于早期的局限性 PCa ;对于中晚期 PCa ,需结合外放疗、 内分泌等治疗。Kucway 等报道 ,对前列腺体积过大或高危病例术前采用雄激素阻断疗法缩小前列腺、降低分期后再行放射性粒子治疗 ,效果满意。107 例患者平均年龄 69 岁 ,前列腺体积 > 50 cm3,经过内分泌治疗后 ,82 %患者前列腺体积缩小到插植放疗的适应标准以下(50 cm3) ,在平均 319 个月的时间后前列腺体积平均缩小达 33 % ,其中激素阻断治疗前的前列腺体积和治疗时间长短是体积缩小程度的 2 个重要因素。PCa 的放疗疗效还有待进一步提高。文献报道 ,PCa 放疗后又出现了其他部位的继发性肿瘤 ,这说明目前所实行的各种放疗措施需要更深入的研究。随着分子生物学技术的快速发展及对放射诱导细胞损伤机制的更深入认识 ,放射治疗结合分子生物学技术 ,必然会产生新的有效的治疗技术 ,如基因替代治疗、 免疫治疗等。PCa 放疗的近期并发症主要为直肠和泌尿系统的毒副反应 ,远期并发症有直肠和膀胱毒副反应 ,包括直肠出血、 前列腺炎、 直肠或肛门狭窄、 放射性膀胱炎、 尿道狭窄及膀胱挛缩等。尿道狭窄主要发生在经尿道前列腺切除后的患者。部分患者放疗后出现性功能障碍 ,尤其是近距离插植放疗 ,但通常西地那非对其有效。常规外照射剂量 70 Gy 时 ,60 %的患者将出现近期直肠和泌尿系统 ≥2 级毒副反应。适形放疗能更好地保护正常组织 ,降低直肠或膀胱的毒副反应。4 三种治疗方法的比较目前 ,尚无临床研究来比较 PCa 确定性治疗的 3种治疗方案 ,原因之一就是放射治疗和手术治疗方法的不断进步。支持 PCa 根治术的学者认为 ,手术可以改善患者局部症状 ,包括出血、 疼痛和尿路梗阻 ,改善患者生活质量。因此 ,不良反应和患者的意向性是决定方案的主要因素。一项回顾性研究报道 ,60 000例局限性 PCa 患者接受 RP ,EBRT 或观察治疗 ,对于高级别的 PCa ,RP显示出更好的 10 年疾病相关生存率。由于多数局部晚期 PCa 是高级别肿瘤( > 60 %) ,这项研究也提示 ,手术治疗可以作为高危人群的确定性治疗方案。推荐放疗( > 70 Gy)或者放疗 +内分泌治疗(如果可以耐受) 。如果发生包膜侵犯 ,则 PCa 根治术较难保证其前列腺切缘阴性 ,然而 ,如果只有少量肿瘤突出在前列腺包膜外 ,则推荐 PCa 根治术。5 展望回顾一下近半个世纪 PCa 治疗的历史 ,可以看到以下的现象:由于 PSA 的应用 ,早期 PCa 的确定性诊治成为了治疗的主流;由于新的技术如机器人手术、 质子放疗的开展 , PCa 的手术治疗进入了新的阶段。但是 ,尚缺乏几种确定性治疗的 “头对头” 比较 ,而且对于一些如 T3 期 PCa 治疗还存在争议。随着 PCa 研究的深入 ,这些问题必将得到更好的解答。【参考文献】[ 1 ] J emal A , Siegel R , Ward E , et al . Cancer statistics , 2006 [J ] .CA Cancer J Clin , 2006 , 56 (2) : 1062130.[ 2 ] Ward J F , Slezak J M ,Blute M L , et al . Radical prostatectomyfor clinically advanced (cT3) prostate cancer since t he advent ofprostate2specific antigen testing 152year outcome [ J ] . BJU Int ,2005 , 95 (6) : 7512756.[ 3 ] Carver B S ,Bianco F J J r , Scardino P T , et al . Long2term out2come following radical prostatectomy in men wit h clinical stageT3 prostate cancer [J ] . J Urol ,2006 , 176 (2) : 5642568.[ 4 ] Freedland S J , Partin A W,Humphreys E B , et al . Radical Pros2tatectomy for Clinical Stage T3a Disease[J ] . Cancer , 2007 ,109 (7) :127321278.[ 5 ] Hill J R , Fine S W , Zhang J , et al . Radical prostatectomy forclinical T3 disease :expanding indications while optimizing cancercont rol and quality of life. Nat [J ] . Clin Pract Urol ,2007 ,4 (8) :4512454.[ 6 ] Musch M , Klevecka V , Roggenbuck U , et al . Complications ofpelvic lymphadenectomy in 1 , 380 patient s undergoing radicalret ropubic prostatectomy between 1993 and 2006 [ J ] . J Urol ,2008 ,179 (3) :9232928.[ 7 ] Martí nez2Salamanca J I , Romero Otero J . Critical comparative a2nalysis between open , laparoscopic and robotic radical prostatec2tomy : perioperative morbidity and oncological result s ( Part I)[J ] . Arch Esp Urol ,2007 , 60 (7) :7552765.[ 8 ] Joseph L ,Chin , Pat rick P. Luke , et al . Initial experience wit hrobotic2assisted laparoscopic radical prostatectomy in t he Canadi2an healt h care system[J ] . CUAJ ,2007 ,1 (2) : 972101.[ 9 ] Pilepich M V , Winter K, Lawton C A , et al . Androgen sup2pression adjuvant to definitive radiot herapy in prostate carcino2ma2long term result s of Phase ⅢRTOG 85231 [J ] . Int J RadiatOncol Biol phys , 2005 , 61 (5) :128521290.[ 10 ] Slater J D , Rossi C J , Yonemoto L T , et al . Proton t herapy forprostate cancer : The initial Loma Linda University experience[J ] . Int J Radiat Oncol Biol Phys , 2004 ,59 (2) :3482352.[ 11 ] Wakat suki M , Tsuji H , Ishikawa H , et al . Quality of Life inMen Treated wit h Carbon Ion Therapy for Prostate Cancer [J ] .Int J Radiat Oncol Biol Phys , 2008 , 72 (4) : 101021015.
施国海 主任医师 复旦大学附属肿瘤医院 泌尿外科3266人已读 - 精选 中国应用舒尼替尼治疗晚期肾癌的IV期临床结果
肾细胞癌为泌尿系常见肿瘤,病理类型以透明细胞癌为主,占肾癌的80%~85%。对肾透明细胞癌von Hippel-Lindau(VHL)综合征的研究,带动了肾癌靶向治疗药物的研发。近7年FDA批准了6种治疗晚期肾细胞癌的靶向药物,分别为舒尼替尼(Sunitinib)、贝伐单抗(Bevacizumab)+α干扰素、帕唑帕尼(Pazopanib)、替西罗莫司(Tersirolimus)、依维莫司(Everolimus)和索拉非尼(Sorafenib)。这些分子靶向药物的作用靶点涵盖血管内皮生长因子(vascular endothelial growth factor,VEGF)、血管内皮生长因子受体(vascular endothelial growth factor receptor,VEGFR)和mTOR等。目前经国家食品药品监督管理局批准用于晚期肾癌的靶向药物仅有舒尼替尼和索拉非尼。中国医生发现舒尼替尼和索拉非尼使晚期肾癌患者明显获益,但晚期肾癌患者对此两种靶向药物的反应与西方人群似乎存在差异。2011年ASCO年会上 J. Garcia-Donas等报道了西班牙泌尿生殖肿瘤组的一项多中心、前瞻性研究,初步探讨100例索坦一线治疗患者的基因多态性与舒尼替尼疗效及副反应的关系,初步发现VEGFR3单核苷酸多态性与舒尼替尼一线治疗肿瘤进展时间(TTP)有相关性,CYP3A5单核苷酸多态性可能与3/4级副反应存在相关性[1];T. Mizuno等报道ABCG2 421基因型可能与药物暴露相关,ASCG 421C>A多态性可能引起舒尼替尼药物暴露量增高以致副反应发生率增高[2],。均提示可能存在基因型差异导致个体对多靶点酪氨酸激酶抑制剂(tyrosine kinase inhibitor,TKI)疗效和副反应的不同。中国尚无此类报道,目前仅从以下中国学者总结的临床靶向治疗数据初步探讨中国晚期肾癌患者靶向治疗结果与西方研究的差异。一、 舒尼替尼治疗中国晚期肾癌患者疗效与西方研究结果比较2011年中国泌尿外科学会年会上,舒尼替尼治疗中国晚期肾癌IV期临床研究第二次中期分析结果公布。该研究是国内目前最大的单药治疗晚期肾细胞癌的前瞻性、开放性、单臂、多中心研究,证据级别较高。共入组105例患者,治疗持续时间平均达244.7d(标准差173.8),近9个用药周期。获得部分缓解(PR)31例(30.1%),客观缓解(ORR)为32例(31.1%);临床控制率(DCR)为76.9%;中位无病生存期(PFS)13.5个月,比西方舒尼替尼一线治疗晚期肾癌III期研究11个月[3-4]更长。数据分析截止时,<50%的患者死亡,中位总生存期(OS)未达到。何志嵩等[5]报道了舒尼替尼治疗37例晚期肾癌患者的结果。其中一线治疗30例,细胞因子或索拉非尼治疗进展后二线治疗7例,获得部分缓解(PR) 9例(26.5%),稳定(SD)24例(70.5%),疾病进展(PD) 1例(3.0%),DCR为97.0%。中位随访时间达到12个月时仍有62.5%患者无疾病进展,中位PFS未获得。施国海等[6]报道舒尼替尼治疗晚期肾透明细胞癌45例,获得DCR 80%,中位PFS 11个月。对于转移性非透明细胞癌患者,舒尼替尼治疗肾乳头状癌、嫌色细胞癌、集合管癌有效,对淋巴结转移及肺转移的患者疗效较好[7]。日本II期临床研究结果:舒尼替尼一线治疗中位TTP 12.2个月,二线治疗中位TTP 10.6个月[8],优于西方研究。因此从中国大部分数据和日本研究来看,索坦似乎对亚洲患者疗效更优,而靶向治疗因为人种差异导致疗效差异在肺癌中已经证实,在肾癌中不能除外。中国食品药品监督局(SFDA)批准舒尼替尼治疗晚期肾癌,中国版NCCN肾癌治疗指南推荐索坦用于晚期肾癌的一线治疗。二、 舒尼替尼治疗中国晚期肾癌患者副反应与西方研究结果比较中国舒尼替尼治疗晚期肾癌IV期临床研究中未出现与III期研究[3-4]中不同的副反应,大部分副反应发生率与III期研究[3-4]类似,而以下四项副反应发生率要高于III期研究:手足综合征(62.9% Vs. 29.0%)、高血压(37.1% Vs. 30.0%)、甲状腺减退(24.8% Vs. 14.0%)、血小板降低(74.3% Vs. 68.0%)。IV期研究第二次中期分析时,8.0%的患者由于不良事件退出研究,因不良事件减量的患者比率为29.5%,低于国外III期研究[4]的19.0%和32.0%[5]。国内单中心病例总结结果与西方研究结果比较,舒尼替尼在高血压、手足皮肤反应、甲状腺功能减退和血小板减少较西方研究发生率要高[5-7]。日本报道的舒尼替尼II期研究中[8],舒尼替尼因副反应停止治疗率为25%,明显高于西方研究[4],且在这项II期研究[8]中均观察到血脂升高发生率>50%,较西方研究[4]高,但此副反应在国内病例总结中未提及。总体来讲,舒尼替尼在中国患者的副反应谱与西方研究类似,某些发生率较西方研究明显增高。副反应从临床观察各有特点:以血液学副反应为主,血小板减少为中断治疗和减量主要原因。舒尼替尼有高血压副反应,因此有心脑血管高危风险的患者在使用此药物时均应严密监测血压。临床医生应根据患者情况全面评估选择药物治疗。三、 肾癌靶向治疗展望个体化靶向治疗是各种肿瘤治疗发展的趋势。根据患者基因情况选择适合的靶向治疗不但可以让患者更多获益、更少承受副反应,还可能为患者减少经济负担。在暂时还不能实现基因个体化治疗的今天,我们应积极根据既往总结的数据去探寻患者的差异。例如目前在肾癌的靶向辅助治疗中,我们无法知道哪些患者会从治疗中受益,而从临床特征我们可以知道同侧肾上腺受侵或转移和肿瘤侵及肾周筋膜患者5年肿瘤特异性生存率<25%[10-13],肿瘤侵及腔静脉或区域淋巴结转移5年肿瘤特异性生存率则在30%左右[14-21],与远处转移性肾癌患者5年肿瘤特异性生存率(20%左右[14])类似;肿瘤坏死、大小、分化程度、病理类型等均与患者预后相关[20]。因此对于此类高危患者术后则给予靶向辅助治疗进行临床研究。
施国海 主任医师 复旦大学附属肿瘤医院 泌尿外科3768人已读 - 精选 微创治疗肾癌前列腺癌----路在何方
微创治疗肾癌前列腺癌----路在何方在过去的50年中,由于影像技术的发展,小肾细胞癌即直径小于100px的肾癌的发病率增长了1倍,其在肾癌总的发病率比率也逐年上升,直径小于100px的肾肿瘤20%为良性肿瘤[1]。同时,对肾肿瘤切除术后肾功能减退,全身代谢性疾病的发病率显著增加,保留肾脏手术日益受到关注。尤其对于老年人,围手术期风险较大,微创消融手术如冷冻治疗或射频消融治疗可以作为一个选择。肾癌微创治疗的目的是尽可能保留正常肾组织和尽可能减少并发症。射频消融术和冷冻治疗是目前研究比较多的方式[2],本文就这两种微创治疗技术进行了讨论。1997年,Zlotta等[3]首次报道在行根治性肾切除术前一周行经皮射频消融治疗位于外周的肾肿瘤,1999年又进行了动物试验方面的研究。同年,McGovern等[4]在超声引导下为1例拒绝外科手术的肾脏肿瘤患者成功施行了射频消融治疗。多数研究者把射频消融治疗技术作为一种姑息手术,应用于不能手术或不能耐受手术,或拒绝手术的肾癌患者。2011年NCCN肾癌治疗指南中指出:对于无法耐受手术的T1期肾脏肿瘤可以选择主动监测或者消融治疗,热消融治疗后肿瘤局部复发的风险要高于传统手术。而在2011年EAU肾癌治疗指南中,经皮微创消融技术,作为2b类证据用于肾脏肿瘤治疗。其优势在于减少围手术期并发症,无需入院治疗,并且能够降低高危患者的手术风险。适应证为小的、偶发于肾脏皮质的老年患者,具有肿瘤的高度易感性的患者,双肾肿瘤,孤立肾术后可能发生肾失功的患者。绝对禁忌征包括凝血功能障碍,危重病人等。技术信息1、射频消融术原理 利用频率为460~500 KHz的高频交流电,通过150~200 W的射频发生仪和与其连接的针形射频消融电极,插入靶组织内,后尖端产生热能从而消灭肿瘤细胞。敷于患者大腿的分散电极与消融电极形成电流回路。活体组织细胞在49 ℃时数分钟内即可死亡,超过60 ℃则可引起细胞蛋白变性,酶功能丧失,胞膜溶解,细胞质被破坏导致不可逆性死亡。电极有单极和多极之分,单极射频消融针一次治疗肿瘤的范围较小,多极电极针展开后成伞形、椭圆形等,增大了治疗范围。在影像设备导向下的经皮射频消融术实用性强,肾功能欠佳者也可行此法治疗。2、冷冻消融术原理 冷冻消融术是最早在临床应用的温度治疗方法,应用较广泛。液氮或氩气使局部温度迅速降至-20 ℃或以下,通过低温、冷冻和热融3个过程使细胞变性、崩解和死亡。冷冻消融的机制包括:(1) 组织内的温度降至-50~-60 ℃,细胞内形成的冰晶通过机械损伤可直接导致细胞死亡;(2) 细胞间隙内形成的冰晶,使细胞外液浓缩,细胞脱水,皱缩;(3) 细胞内液的电解质浓度升高,酶的活性下降促使细胞中毒损伤;(4) 组织冷冻后,小血管收缩,毛细血管迅速闭塞,微循环停止,细胞由于缺血而死亡(5)冷冻术后,细胞碎裂,肿瘤抗原释放,引发后续免疫反应。因为肿瘤边缘易残存,往往需要对其周围1 cm 以上的正常组织进行冷冻以防肿瘤细胞残存。数次冷冻解冻过程较一次冷冻治疗效果好。影像学定位目前没有大宗的临床试验比较超声,CT和MRI应用在消融术上的差异,每一种方式都有其优势和劣势。超声的优势在于可以实时的监视肿瘤,但是超声对于操作者的依赖性较强,受干扰因素较多,如患者体型过大,肠胀气等。CT则较少受到干扰,但是图像质量可能受到影响。通过增强CT可以将凝固坏死后的肿瘤和正常的组织区分。MRI则以软组织作为对比,通过不同序列图像对肿瘤进行定位。快T1加权像T2序列不但能够实时定位,还能够对消融术后疗效进行实时的监控。对于冷冻消融治疗,由于肿瘤内各点温度的差异,为了保证切缘充分,冷冻范围必须包括肿瘤外5 mm正常肾组织,由于冷冻后冰结晶可能产生声影,超声无法明确其边界,借助CT可避免其他组织副损伤,而MRI则可以通过T1加权的信号变化看到这个密度减弱条带,明确消融后切缘的情况。手术方式射频消融和冷冻治疗都可以采用经皮方式或者腹腔镜手术方式。以往射频消融多采用经皮方式,而冷冻治疗则多采用后者。随着微管化技术的进展,冷冻治疗也逐渐过渡到经皮方式。一般来说,肾脏腹侧面的肿瘤不适合经皮方式,但这并不是决定的禁忌症。Finley[5]比较经皮和腹腔镜冷冻治疗肾癌的疗效,结果显示无论是手术时间还有住院时间,后者均较经皮方式延长。经皮方式探针数目应用更少,麻醉时间更短,住院时间更短,恢复更快,手术并发症也更少(3% & 7%)。射频消融也呈现类似的特点。腹腔镜下手术创伤较经皮路径大,但因是在直视下操作,有治疗较彻底的优点。有报道,腹腔镜下及经皮治疗后需再次治疗的比率分别为5.1%和27.5%。解剖及肿瘤因素Gervais等[6]学者对100例应用经皮肾脏穿刺患者多因素分析发现肿瘤的大小和位置是预测RF消融的独立因素。肿瘤大小(<3 cm)及肿瘤位置(周围型),位于外侧及后侧的肾细胞癌比位于内侧及前侧者更易于治疗。对于<3 cm的肾细胞癌,其完全坏死率可达100%,3~5 cm肿瘤坏死率约93%,>5 cm时坏死率则约为28%。血管内血流的冷却作用以及组织的电阻作用可影响射频消融术的治疗范围。对缺血组织及无血管组织进行射频消融术可增大其治疗范围。血管进行栓塞后可以增加射频治疗疗效。因为肾周脂肪的绝缘性和大血管的散热作用,周围型肾癌常出现完全坏死。而中央型肾癌则不同,过热导致集合系统和肾窦大血管的损伤。尤其注意肾脏和周围脆弱的组织,如输尿管,生殖股神经和髂腹股沟神经,腰大肌,小肠及回肠,肾上腺。物理因素肾脏是高灌注的器官,其灌注量是肝脏的四倍,这个特点决定其散热方式以及能量损耗的差异。由于大血管的灌注,“热消退”效应可能削弱对肿瘤治疗的能量,因此,对于高灌注的肾肿瘤,可以考虑增加消融的次数,或者减慢射频消融后温度降低的速度。与冷冻治疗相比,射频消融术后肿瘤术后复发需要再次消融的比例相对较高。肿瘤特征及病人选择术前CT或者MRI检查确定肿瘤临床分期,为了达到根治效果,肿瘤一般为T1-T3a或者Robson分级I或II期。对于晚期肾癌,可以应用消融技术局部治疗肿瘤或者减轻疼痛和血尿症状。对于囊性肾癌,研究较少,Park等[7]学者应用射频消融治疗9例Bosniak分级为III级到IV级的患者,随访8个月未见复发。目前一般认为对于肿瘤较小(<75px< span="">)的囊性肾癌比较适合。并发症 射频消融术治疗肾细胞癌的安全性至少与肾部分切除术等同。并发症包括肾功能损伤及操作相关并发症。Hegarty等[8]对82例应用经皮射频消融术治疗肾细胞癌患者进行研究,2年肾功能随访显示无变化。对孤立肾的治疗同样是安全的。主要并发症指需要进行临床治疗,否则可能出现永久性的不良反应或坏死等并发症,包括大出血、输尿管损伤、尿瘘、结肠损伤、肾肠瘘和严重气胸等[9]。射频消融术所致大出血(需要输血)的发生率为0~2%[10-11]。次要并发症基本可以保守治疗,主要包括疼痛,少量出血/血尿,术后泌尿系感染,伤口感染,神经肌肉损伤及血肌酐轻度升高等。总体而言,主要并发症的发病率远低于次要并发症的发病率。肿瘤与周围脏器的距离与并发症发生率密切相关,同时与操作者经验亦有关联。有多中心研究显示,小肾细胞癌经皮射频消融术主要并发症发生率为11%,而并发症的一半发生于早期1/3操作中,提示其与学习曲线有关[12]。消融术前病理以往多数学者认为经皮肾肿块穿刺存在取样误差,假阳性等问题,即使穿刺结果准确,肿瘤多为早期肿瘤,术后多无需辅助治疗,因此经皮肾脏肿块穿刺病理诊断意义不大。但是随着消融技术的广泛应用,确定性病理诊断对于判断其疗效尤为重要,以往的研究仅从影像学诊断的肾肿瘤进行微创治疗来判断其疗效,由于其中有些是良性的血管平滑肌脂肪瘤,其疗效可能被高估,或者存在过度治疗。有学者对肾肿瘤应行穿刺活检[1],结果表明,37%的患者穿刺结果为良性。因此建议微创治疗前穿刺取病理,这对于患者的诊断和以后的随访治疗具有重要意义疗效评估 射频消融术的疗效与肿瘤大小及位置密切相关,研究显示在单次治疗中影响肿瘤完全凝固坏死的因素包括:肿瘤大小(≤3 cm)及肿瘤位置(周围型),位于外侧及后侧的肾细胞癌比位于内侧及前侧者更易于治疗。Zagoria等[13]对104名患者的125个0.6~8.8 cm肾细胞癌行射频消融治疗,平均随访时间13.8个月,其中116例肾细胞癌完全消融。95例直径<3.7 cm的肿瘤消融完全,30例直径>3.7 cm的肿瘤中21例发生部分坏死,9例随访中发现有残瘤。对T1a期肿瘤直径<4 cm的肾细胞癌而言,射频消融术1年及2年无瘤生存率近似或明显优于部分性肾切除病例。Stern等[14]将射频消融术与部分肾切除术进行随机对照(针对T1a期肾细胞癌),射频消融术和部分性肾切除术3年的无瘤生存率分别为93.4%和95.8%,差异无统计学意义。Hakime等[16]在裸鼠中做试验证实射频消融术联合抗血管生成药sorafenib可以有效降低微血管密度,扩大射频诱导的凝固性坏死区域。Arima等[17]报道了对31例T1N0M0肾细胞癌患者行2期射频消融治疗,其中29例患者在进行动脉栓塞瘤血管6 d后行射频消融治疗,随访2年局部控制率达100%(包括1例肿瘤直径>4 cm复发又行射频治疗的患者)。据Zagoria等[18]报道了320例肿瘤直径为2.3~2.6 cm肾细胞癌接受冷冻消融术治疗的疗效,在5.9~72.0个月的随访期间,其生存率为97%~100%。另有综述报道326例病例,随访时间为30.8个月,其肿瘤复发率为4.6%,其并发症发生率为10.6%。对较大肾细胞癌而言,冷冻消融术疗效优于射频消融术。因射频消融术治疗肾癌的临床应用晚于冷冻消融术,尚待进一步研究。前列腺射频及冷冻消融研究前列腺癌作为较常见的老年性恶性肿瘤已构成对人类生命的威胁。尽管我国前列腺癌发病率远低于欧美国家,但随着国人平均寿命的延长,诊断技术的提高,尤其是前列腺特异性抗原(prostate specific antigen,PSA)检测的广泛应用,前列腺癌的检出率也显著上升。前列腺癌有多种治疗方法,包括手术、内分泌治疗、放射治疗等。对局限性前列腺癌的治疗,目前临床上以根治术和主动监控为主。然而根治术的创伤较大,带来的并发症较多,影响生活质量,并且由于前列腺癌患者年龄多较大,合并其他老年性疾病的机会较多。主动监控后前列腺癌的病理分期分级的增高导致前列腺癌病人不愿采用主动监控。前列腺癌射频消融治疗的出现适应了这部分患者的需求。射频消融在前列腺上的应用可追溯到20世纪90年代初,最早开始于对前列腺增生的研究[19]。Djavan等[20]和Zlotta等[21]首先报道应用射频消融技术治疗前列腺癌。该手术可在全麻、腰麻或局部麻醉下进行,患者取截石位。应用三腔导尿管灌注生理盐水来冷却尿道。在经直肠超声引导下将三钩状子针单电极经会阴插入前列腺内,这样可产生一个可预知的球形凝固灶。每一个钩状子针都有热电偶,可控制组织内的温度达到且维持在所需水平。治疗的目的是每一个子针在2~3 min内达到 100℃并维持此温度水平达3 min。Djavan等[22]对21个前列腺射频消融灶的MRI与组织病理做了相关性研究,认为射频消融是一种安全、可行的方法,病灶大小位置可预测。消融灶MRI观测与组织病理学的凝固性坏死灶有很好的相关性。Zlotta等[23]对15例拟行前列腺根治术患者进行了组织病理学研究以评价射频消融的安全性和可行性。手术耐受性好,无并发症报道。随后不少国内外学者都对超声引导下经会阴径路射频消融治疗前列腺癌进行了基础和临床研究。研究结果认为射频消融可有效治疗局限性前列腺癌,消融后前列腺体积缩小,PSA明显下降,穿刺活检病理消融区域呈凝固性坏死。这些表现与消融灶的大小、前列腺癌灶的灭活程度、肿瘤分期、随访时间、有无同时行内分泌治疗、放疗等有关[24-26]。PSA下降值与消融范围密切相关,双侧消融优于单侧消融,单侧整体消融优于单侧区域消融。但B期以上病例PSA会出现反弹。经直肠彩色血流超声和(或)灰阶实时超声谐波造影未见明显异常者,可作密切随访观察。如动态观察逐步明显升高要寻找原因,如增强造影局部有异常可以考虑重复消融治疗或配合其他疗法[27]。从现有经验来看,超声引导下前列腺癌射频消融主要适合于局限性前列腺癌患者;或存在手术禁忌证以及无法耐受手术的患者;内分泌或放疗治疗失败者等。但是与其他实质脏器肿瘤射频消融不同,射频消融技术治疗前列腺癌在经过近十几年的发展后,仍然处于探索性阶段,未能在临床上得到广泛的应用。制约其在前列腺癌临床应用可能有以下原因: (1)前列腺解剖特殊,射频消融过程中容易造成前周边结构受热损伤,造成术后严重并发症。(2)前列腺癌多灶性[28-29]及多样性的特点增加了治疗手术和疗效评价的难度。目前多需通过对整个腺体进行消融及系统性治疗以达到更好的疗效。(3)前列腺癌患者往往合并有前列腺增生,部分患者前列腺体积增大明显、形态失常,造成布针点数增加、增加重叠布针困难。(4)射频消融凝固灶虽可预测,但是消融灶大小、形态受血流灌注等诸多因素影响,导致热量在靶区分布不均,容易造成治疗不彻底。(5)目前的技术现状而言,尚未开发专门用于前列腺的射频消融电极,前列腺射频消融的热场研究和前列腺特定形态的适形消融问题尚未进行深入研究。目前,治疗前列腺常采用凝固灶为球体或椭球体的电极,这样的电极无论是从重叠布针的技术难度还是从手术安全性而言,均制约着射频消融在前列腺的应用。冷冻治疗前列腺癌也开始于上世纪90年代,前列腺部位达到<-40 ℃,周围组织如直肠外括约肌则保证温度,避免损伤。最初是直径3mm的探针,随着技术的改进,1.5mm,即17 G的探针逐渐采用。冷冻治疗要达到两点:1,诱导细胞死亡,包括冷冻破裂、坏死和凋亡。2,最大的杀伤细胞,涉及冷冻速率,目标温度,冷冻时间,复温时间,冷冻循环数等等。目前对于低中危的局限性前列腺癌,前列腺的大小也是重要的因素之一,对于过大的前列腺,可以考虑新辅助治疗如内分泌治疗,但是结果尚不明确。对于PSA>20ng/ml 或者GS 8到10分的患者,盆腔淋巴结转移的风险增加,因此通过nomograms或者其他已经肯定的预测办法判断出淋巴结转移的概率在25%以上的患者建议在冷冻治疗前明确盆腔淋巴结是否转移。既往有过TURP手术病人不建议冷冻治疗,冷冻会导致尿道坏死风险增高,粘膜加温困难,进而腐肉形成,尿潴留风险增加。因此一般建议PSA<10 ng/ml的患者应用冷冻治疗。对于Gleason score 7到8分,PSA>10 ng/ml 但是<20 ng/ml,或者临床分期T1b的患者可以采用冷冻治疗。冷冻治疗的疗效采用监测PSA变化和消融术后穿刺活检的病理诊断,目前尚缺乏一致的生化复发的标注,因为尿道保留,因此冷冻术后可能PSA无法降到很低水平,但PSA的谷值越低,术后前列腺活检阴性可能性越低,PSA稳定时间越长。目前已有的文献报道[31-33],低中高危前列腺癌五年生化复发的风险分别为65%~92%,69~89%,48~89%。按照ASTRO标准即PSA连续三次升高,低危患者5年无疾病复发率为85%,中危和高危分别为73.4%和75%。而应用Phoenix标准即PSA最低点加2,低危中危高危的5年无生化复发比率分别为91%,78%和62%。尚缺其它一些长期随访的结果,如转移情况,疾病特异性生存时间,因此尚无法与前列腺癌根治术与放疗的结果进行比较。术后一般6~12月内根据PSA的情况决定是否需要前列腺活检。文献报道活检阴性率较高,87~98%。当然,活检阴性并不代表肿瘤完全消失,正如前列腺癌放疗一样,活检阴性只是说明治疗失败的可能性下降。短期的并发症包括阴囊阴茎水肿,腺体水肿,阴茎麻木等,多可自愈。长期的并发症包括尿道瘘,尿失禁,勃起功能障碍,尿道腐肉形成。也有学者尝试前列腺癌挽救性冷冻治疗[34-36],适应症为PSA<4 ng/ml,PSA倍增时间较长,没有精囊侵犯,预期寿命10年以上,无远处转移。目前尚缺乏挽救性冷冻治疗前内分泌治疗能够获益的报道,但内分泌治疗可以缩小前列腺体积。一般认为再次活检阳性或者PSA持续上升大于0.5 ng/ml一般认为治疗失败。有学者应用两循环治疗后,再次活检阴性率为93%,无生化复发生存率为66%。术前PSA>10或者Gleason score>=8分,常预测治疗失败。Bahn报道7年挽救性冷冻治疗后无生化复发率,以PSA<0.5 ng/ml 为59%,PSA<1 ng/ml为69%。Ghafar等学者报道PSA谷值<0.1 ng/ml,1年和2年的五生化复发率为86%和74%。当然挽救性治疗术后尿道瘘等发生率会显著增高,这些效果伴随的是巨大的并发症风险。结论目前,上述技术在治疗肿瘤方面还处于起步阶段,一系列初步临床应用都是在选择性病例中使用,研究的样本量较小,报道的文献数目也很有限,且研究结果大都是基于影像随访结果,随访期均较短,远期癌肿控制率仍未确定。不同的研究其具体治疗步骤、技术成功率、并发症以及结果具有一定差异,肿瘤的大小和治疗时间、治疗参数之间的关系重复性不好,所以还需进行进一步的多中心临床试验以观查微创治疗技术在治疗肾癌患者5年以上长期生存率结果。微创治疗的选择仍需要十分谨慎,需要充分考虑到患者的意愿,肿瘤的相关因素,技术的差异性和随访的多样性。实体肿瘤的微创治疗是现代医学发展的一个总的趋势,射频消融技术作为其中重要一种在未来几年必会有更快的发展,而治疗的安全性和有效性也将是更多学者关注的重点。对肾、前列腺而言,在参考肝脏射频消融经验的同时,要结合脏器自身特点,进行更深入的基础和临床研究,使该技术能更好的服务于临床诊疗。众多研究表明随着微创治疗设备的不断改进,术中监测技术的逐步提高,操作经验的日趋成熟,微创治疗技术将在肾癌前列腺癌治疗领域中发挥越来越大的作用。参考文献,篇幅限制略。
施国海 主任医师 复旦大学附属肿瘤医院 泌尿外科2709人已读 - 诊后必读 遗传性肾癌家系如何随访?施国海 主任医师 复旦大学附属肿瘤医院 泌尿外科1342人已读
- 诊前须知 疫情期间索坦慈善赠药新规定
【中国癌症基金会索坦英立达项目办公室】尊敬的项目指定医生,您好!鉴于疫情的特殊性,为确保入组患者的健康和安全,即日起至2月29日期间对于无法去医院随访的患者,项目启动特殊预案即:不强行要求患者去医院随访,患者可就病情和用药的安全有效自行电话与您进行沟通,并在得到您认可后提交相应情况说明,关于说明的具体内容或其它任何问题,请患者拨打咨询热线:010-67770237。感谢您的付出,疫情期间请做好防护!
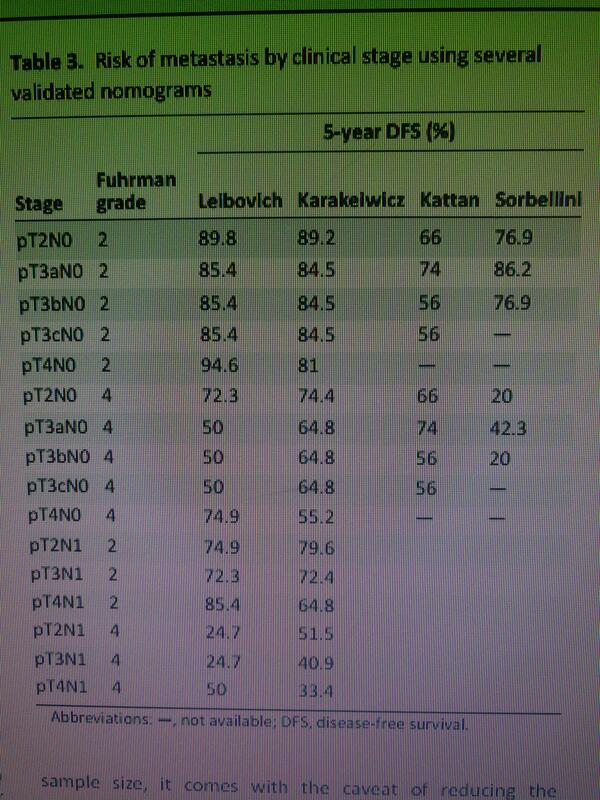
施国海 主任医师 复旦大学附属肿瘤医院 泌尿外科2128人已读 - 诊后必读 肾癌术后五年无复发率风险表
肾癌术后五年无复发率
 施国海 主任医师 复旦大学附属肿瘤医院 泌尿外科3279人已读
施国海 主任医师 复旦大学附属肿瘤医院 泌尿外科3279人已读





